虽然还没有商业化产品,但对药物领域有着高研发投入寄望于为人类健康“攻坚克难”,这是因明生物的理想。
众所周知,关乎人类福祉的生物医药行业,不少公司在研发阶段可谓豪掷重金,从而大幅亏损。所以,一定阶段后,这样的公司往往选择去冲刺资本市场,由公众投资者来继续支撑着公司的药物科研梦。
因明生物就是这样一家公司,它如今正把融资目标放到了香港资本市场。
 (相关资料图)
(相关资料图)
8月17日,广州因明生物医药科技股份有限公司(以下简称,因明生物)向港交所递交招股书,拟香港主板IPO上市,中金公司、瑞信为其联席保荐人。
01
官网尚需等待中
资料显示,因明生物创立于2019年10月,作为一家创新驱动型的生物制药公司,致力于自主研发的首创新药,来解决全球多个医疗领域尚未获满足的临床需求。目前,因明生物的研发团队有169名人员,其中有着多名潜心钻研免疫治疗、眼科药物等领域的科学家。该公司拥有一条产品管线和一款核心产品。这条产品管线主要包括七种在研药物,涵盖眼科药物、重组蛋白肉毒素、小分子免疫药物和细胞治疗等。其核心产品名为”QA102“,主要用于治疗干性年龄相关性黄斑变性。
截至2022年8月11日,因明生物的产品管线主要包括七种在研药物,各项在研药物均为自主研发,涵盖眼科药物、重组蛋白肉毒毒素、肿瘤免疫药物以及宠物免疫药物四大领域。
《港湾商业观察》试图打开因明生物官网,但其只能看到一张关于公司介绍的说明,其他则无法打开,官网称,“更多内容,敬请期待”。
有港股投资人士向《港湾商业观察》表示,“对于递表的企业而言,招股书和官网都是投资者查阅或联系公司的重要渠道,如果官网无法打开,则多少说明公司准备工作有所不足,毕竟,投资者都希望可以了解更多公司的发展,招股书可以参考,官网则往往代表了一家公众公司的重要招牌或门面。不过,这类情况也不少见。”
02
净亏损超13亿元
财务数据层面,2020年、2021年及2022年前4个月,因明生物的其他收入分别47万元、168.2万元、148.6万元;净利润分别为-1.73亿元、-7.69亿元、-4.17亿元,累计亏损为13.59亿元。
报告期内,因明生物按公平值计入损益的其他金融负债的公平值变动亏损分别为1.03亿元、4.67亿元、3.11亿元。
在非国际财务报告准则下,因明生物的经调整净亏损分别为6970.2万元、2.21亿元和9571.2万元,累计为3.86亿元。
针对亏损原因,因明生物介绍,绝大部分亏损由其研发开支产生的成本、行政开支及其他金融负债的公平值变动亏损导致。
据悉,在报告期内,因明生物的研发开支分别为6090.8万元、2.26亿元和8973.5万元,CRO开支与员工成本是因明生物研发开支的主要支出项目,二者合计占公司研发总开支的比例分别高达77.95%、60.02%、72.12%。因明生物目前的研发团队有169名成员,其中164名雇员位于中国,另外5名雇员位于美国。
企查查显示,因明生物目前已经融资到A+轮,而2021年公司就进行了2轮融资,分别是2021年3月融资金额为6000万美元,9月融资金额为5000万美元,两轮融资的投资机构包括高榕资本、横琴金投、境成资本、华金资本等。
融资是为了发展,亏损同样也是为了更好发展。而在眼科领域拥有一定研发技术的因明生物,上市前无疑得到了资本市场的认同。
国泰君安研究认为,近年来,中国眼科患病率不断增加,但诊断率较低,大量眼科患者需求尚未被满足。眼科药物虽然技术壁垒较高,但随着新药和新技术的不断创新突破,我国眼科用药市场规模有望进一步壮大,该领域前景广阔。
03
市场前景虽好,商业化转化能否实现?
“眼科是研究发生在视觉系统,包括眼球及与其相关联的组织有关疾病的学科,眼病一般可根据发病位置分为眼前和眼后疾病。由于人口老龄化、电子产品广泛使用、用眼强度加大,近年来各类眼病发病率不断呈上升趋势。Frost & Sullivan报告显示,2019年中国的十大常见眼科疾病依次为屈光不正(包括近视、远视及散光)、结膜炎、干眼症、白内障、睑缘炎、视网膜病变、斜视、弱视、青光眼和葡萄膜炎。”
据了解,因明生物的核心产品为QA102,属于小分子在研药物,用于治疗干性年龄相关性黄斑变性。年龄相关性黄斑变性(AMD)是一种导致老年人不可逆视力损伤的严重致盲性眼病。公开资料显示,干性AMD患者占到了AMD患者总数的80%-90%,是导致老年人视力丧失的主要原因之一。该药物为口服药物,因明生物表示,能有效提升患者依从性,且与目前正在临床开发的其他干性候选药物相比,QA102采用了一种独特的作用机制。
然而,现实的问题是,世界范围内尚未研发能防止干性AMD恶化的获批疗法,既说明市场空间巨大,同时也表明难度相当巨大。
根据弗若斯特沙利文报告,预计全球干性AMD市场将由2023年的2.98亿美元增至2025年的16.97亿美元,复合年增长率为138.5%,2030年,这一市场将达到72.7亿美元,复合增长率为33.8%。一旦有效治疗药物获批并商业化,市场将呈爆发式增长。
根据弗若斯特沙利文信息,QA102是由中国公司开发的首个干性年龄相关性黄斑变性并已获美国食品药品监督管理局批准进行临床试验的在研药物。干性年龄相关性黄斑变性全球尚无有效治疗方法,而QA102已于2022年5月在美国开展II期临床试验。
截至目前,除QA102外,全球还有4种已进入II期及以上临床试验的干性年龄相关性黄斑变性小分子在研药物。其中进展最快的是AlkeusPharmaceuticals公司的一款药物,已于2019年2月进入三期临床。在国内,因明生物已向中国国家药监局申请4项药物临床试验申请,其中有3项已获批。
整体来看,因明生物在研产品尚处于前期阶段,距离推向市场以及商业化变现都还有漫长之路,公司目前尚无任何商业化销售的产品。
因明生物在招股书中坦言,生物制药产品的临床开发过程漫长、成本高昂,加上结果不确定,早期研究及早期临床试验结果,也可能无助于预测最终的试验结果。
“我们的业务及财务前景在很大程度上取决于临床阶段及临床前阶段在研产品成功与否。倘若无法成功完成临床开发、获得相关监管批准或实现商业化,或在上述任何方面遭遇重大延误,公司的业务及盈利能力可能会受到不利影响。”公司表示。
有市场人士告诉《港湾商业观察》,拥有核心的技术优势对生物医药公司而言至关重要,因此前期亏损并不是问题,问题是其核心技术优势在全球范围内,是否真正具备?或者说领先同行多久?如果说同行能迅速研发成功,继而转化为商业化,哪怕只晚一步,可能公司的优势就荡然无存,也意味着前期的努力等于白费。
因明生物在技术层面如何与国际同行展开竞赛,商业化变现之路预计还需要多久,其核心竞争力又真正体现在哪些方面,《港湾商业观察》试图就这些问题联系因明生物,未能收到相关回应。(港湾财经出品)

 猜你喜欢
猜你喜欢 播报:3期临床数据惊艳,荣
播报:3期临床数据惊艳,荣  CPI高于预期!美国通胀继续
CPI高于预期!美国通胀继续  今后五年北京经济总量将突破
今后五年北京经济总量将突破  世界新消息丨“金九”落空
世界新消息丨“金九”落空  复星系减持两公司 港股复星
复星系减持两公司 港股复星  前8个月山西省一般公共预算
前8个月山西省一般公共预算  柏厨家居成功斩获华腾杯2022
柏厨家居成功斩获华腾杯2022 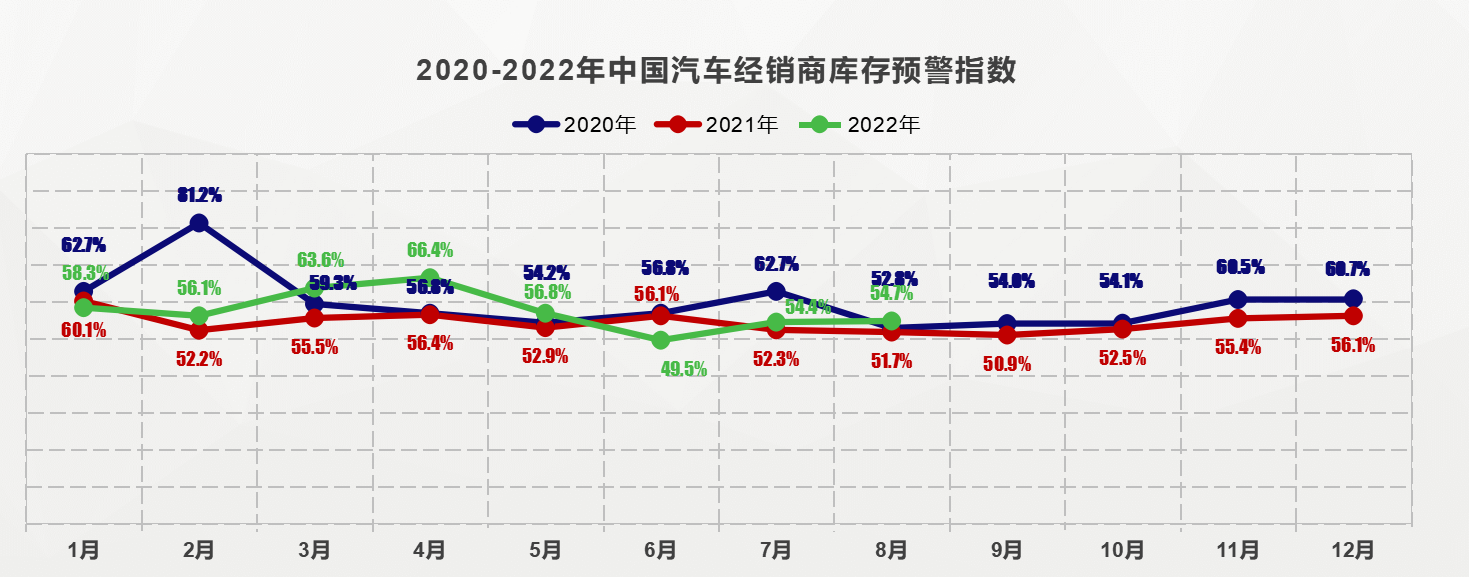 8月库存预警指数表现稳定
8月库存预警指数表现稳定 



